Блок 1. Теоретические основы химии
1.4. Химическая реакция
1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Гидролиз – это взаимодействие веществ с водой, в результате которого изменяется среда раствора.
Катионы и анионы слабых электролитов способны взаимодействовать с водой с образованием устойчивых малодиссоциируемых соединений или ионов, в результате чего меняется среда раствора. Формулы воды в уравнениях гидролиза обычно записывают в виде НОН. При реакции с водой катионы слабых оснований отнимают от воды гидроксил ион, и в растворе образуется избыток Н+. Среда раствора становится кислотной. Анионы слабых кислот притягивают из воды Н+, и реакция среды становится щелочной.
В неорганической химии чаще всего приходится иметь дело с гидролизом солей, т.е. с обменным взаимодействием ионов соли с молекулами воды в процессе их растворения.
Различают 4 варианта гидролиза.
1. Соль образована сильным основанием и сильной кислотой.
Такая соль гидролизу практически не подвергается. При этом равновесие диссоциации воды в присутствии ионов соли почти не нарушается, поэтому рН=7, среда нейтральная.
Na+ + H2O 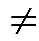 Cl + H2O Cl + H2O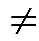
2. Если соль образована катионом сильного основания и анионом слабой кислоты, то происходит гидролиз по аниону.
CO32- + HOH = HCO3- + OH-
Na2CO3 + HOH 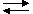 NaHCO3 + NaOH NaHCO3 + NaOH
Так как в растворе накапливаются ионы ОН- , то среда – щелочная, рН>7.
3. Если соль образована катионом слабого основания и анионом сильной кислоты, то гидролиз идет по катиону.
Cu2+ + HOH 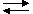 CuOH+ + H+ CuOH+ + H+
СuCl2 + HOH 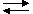 CuOHCl + HCl CuOHCl + HCl
Так как в растворе накапливаются ионы Н+, то среда кислая, рН<7.
4. Соль, образованная катионом слабого основания и анионом слабой кислоты, подвергается гидролизу и по катиону и по аниону.
CH3COONH4 + HOH 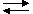 NH4OH + CH3COOH NH4OH + CH3COOH
CH3COO + + HOH 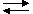 NH4OH + CH3COOH NH4OH + CH3COOH
Растворы таких солей имеют или слабокислую, или слабощелочную среду, т.е. величина рН близка к 7. Реакция среды зависит от соотношения констант диссоциации кислоты и основания. Гидролиз солей, образованных очень слабыми кислотой и основанием, является практически необратимым. Это, в основном, сульфиды и карбонаты алюминия, хрома, железа.
Al2S3 + 3HOH 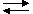 2Al(OH)3 + 3H2S 2Al(OH)3 + 3H2S
При определении среды раствора солей необходимо учитывать, что среда раствора определяется сильным компонентом. Если соль образована кислотой, являющейся сильным электролитом, то среда раствора кислая. Если основание сильный электролит, то – щелочная.
| кислота |
Сильный
электролит |
Сильный
электролит |
Слабый
электролит |
Слабый
электролит |
| основание |
Сильный
электролит |
Слабый
электролит |
Сильный
электролит |
Слабый
электролит |
Среда
раствора |
Нейтральная
рН=7 |
Кислая
рН<7 |
щелочная
pH>7 |
Примерно
нейтральная
рН≈7 |
Пример.
1. Щелочную среду имеет раствор
1) Pb(NO3)2; 2) Na2CO3; 3) NaCl; 4) NaNO3
1)Pb(NO3)2 нитрат свинца(II). Соль образована слабым основанием и сильной кислотой, значит среда раствора кислая.
2) Na2CO3 карбонат натрия. Соль образована сильным основанием и слабой кислотой, значит среда раствора щелочная.
3) NaCl;
4) NaNO3 Соли образованы сильным основанием NaOH и сильными кислотами HCl и HNO3. Среда раствора нейтральная.
Правильный ответ 2) Na2CO3
В растворы солей опустили индикаторную бумажку. В растворах NaCl и NaNO3 она не изменила цвет, значит среда раствора нейтральная. В растворе Pb(NO3)2 окрасилась в красный цвет, среда раствора кислая. В растворе Na2СO3 окрасилась в синий цвет, среда раствора щелочная. |



 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход Поиск
Поиск Друзья сайта
Друзья сайта Наш опрос
Наш опрос Статистика
Статистика

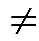 Cl + H2O
Cl + H2O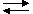 NaHCO3 + NaOH
NaHCO3 + NaOH