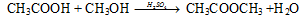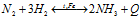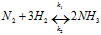| Четверг, 25.04.2024, 21:57 | Главная | Регистрация | Вход |
Сайт учителя биологии и географии Лотоцкой Е. Г. |
|
| Статьи по биологии [132] |
| Статьи по географии [29] |
| Статьи по химии [30] |
| Выступления [3] |
 Поиск
Поиск
 Друзья сайта
Друзья сайта
 Наш опрос
Наш опрос
 Статистика
Статистика

| Главная » Статьи » Статьи по химии |
Существуют обратимые и необратимые химические реакции. Химические реакции, протекающие при данных условиях во взаимно противоположных направлениях с сопоставимыми скоростями, называют обратимыми, например:
В тот момент, когда скорости прямой и обратной реакции выравниваются, устанавливается химическое равновесие, то есть соотношение между продуктами реакций и исходными веществами остается постоянным. Состояние системы, при котором скорость прямой реакции равна скорости обратной, называется химическим равновесием. Такое состояние может сохраняться бесконечно долго, если не происходит изменения условий реакции (концентрации, температуры, давления). При изменении этих условий происходит смещение (или сдвиг) равновесия.
Реакция протекает в газовой фазе, обратима, прямая реакция экзотермична. Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми. При написании уравнений обратимых реакций вместо знака равенства ставят две противоположно направленные стрелки. Уравнение рассматриваемой выше реакции можно записать в виде:
Реакцию, протекающую слева направо, называют прямой (константа скорости прямой реакции k1), справа налево – обратной (константа скорости обратной реакции k2). В обратимых реакциях скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие концентрации исходных веществ, расходуемых на образование продуктов реакции. И наоборот, обратимая реакция в начальный момент имеет минимальную скорость, которая увеличивается по мере увеличения концентрации продуктов реакции. Следовательно, скорость прямой реакции уменьшается, а обратной – увеличивается. Наконец, наступает такой момент, когда скорости прямой и обратной реакции становятся равными. Способы смещения химического равновесия: 1. Увеличение концентрации одного из реагирующих веществ вызовет смещение равновесия в сторону его потребления, так, добавление в систему азота или водорода вызовет сдвиг равновесия вправо, а аммиака — влево. Уменьшение концентрации какого-либо из участников равновесия вызовет его образование. Так, например, связывая аммиак в соль, можно равновесие полностью сместить вправо. Информация с сайта http://netlik.hop.ru/ravnovesie.html | |
| Просмотров: 1562 | Рейтинг: 0.0/0 |
| Всего комментариев: 0 | |


| Лотоцкая Елена © 2024 | Сайт создан в системе uCoz
Некоторые файлы и информация, находящиеся на данном сайте, были найдены в сети ИНТЕРНЕТ, как свободно распространяемые, присланы пользователями сайта или найдены в альтернативных источниках, также использованы собственные материалы. Автор сайта не претендует на авторство ВСЕХ материалов. Если Вы являетесь правообладателем той или иной продукции или информации, и условия, на которых она представлена на данном ресурсе, не соответствуют действительности, просьба немедленно сообщить с целью устранения правонарушения. |
 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход