| Пятница, 26.04.2024, 02:00 | Главная | Регистрация | Вход | |||||||||||||||||||||||||
Сайт учителя биологии и географии Лотоцкой Е. Г. |
|
|||||||||||||||||||||||||
| Статьи по биологии [132] |
| Статьи по географии [29] |
| Статьи по химии [30] |
| Выступления [3] |
 Поиск
Поиск
 Друзья сайта
Друзья сайта
 Наш опрос
Наш опрос
 Статистика
Статистика
Онлайн всего: 1
Гостей: 1
Пользователей: 0

Статьи, выступления
| Главная » Статьи » Статьи по химии |
Агрегатные состояния вещества
Агрегатные состояния вещества
Все окружающее нас вещество находится в одном из трех агрегатных состояний — твердом, жидком или газообразном. В ХХ веке открыли еще одно агрегатное состояние — плазму. Оказалось, что во Вселенной видимое вещество находится преимущественно в состоянии плазмы. Одно и тоже вещество может находиться в любом состоянии в зависимости от окружающих его физических условий. Переход вещества из одного состояния в другое называется фазовым переходом. Испарение, кристаллизация, конденсация и плавление являются примерами фазовых переходов. Идеальный газ
Газом называют агрегатное состояние вещества, в котором молекулы находятся на расстояниях, во много раз превышающих собственные размеры атомов. Свойства газов широко известны: газы легко сжимаются, не сохраняют ни форму, ни объем. Простейшая модель газа описывается следующими свойствами. 1. Газ представляет собой совокупность большого количества молекул. 2. Среднее расстояние между молекулами газа велико по сравнению с размерами молекул. Размерами самих молекул можно пренебречь по сравнению с расстояниями между молекулами. 3. Молекулы газа взаимодействуют друг с другом посредством столкновений. 4. Силами притяжения между молекулами газа пренебрегают. 5. Температура газа определяется средней скоростью молекул. Данная модель газа называется идеальным газом. Модель идеального газа хорошо описывает поведение газов в атмосфере Земли, поведение бензиновой смеси в двигателях внутреннего сгорания и так далее. Оказалось, что модель идеального газа прекрасно работает для объяснения физики внутреннего строения Солнца и других звезд. Средняя квадратичная скорость молекул идеального газа 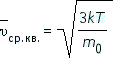 где постоянная Больцмана k = 1,38∙10—23 Дж/К, T — температура газа в кельвинах, m0 — масса одной молекулы. Часто используемое полезное соотношение: 1 а. е. м. = 1,66022∙10—27 кг. Скорости молекул газа были экспериментально определены в опытах Отто Штерна. В пределах погрешности эксперимента они совпали со скоростями, предсказанными моделью идеального газа. Давление газа зависит от концентрации и температуры. Чем выше концентрация газа n (количество молекул в единице объема) и больше температура T газа, тем больше давление газа p = nkT. Другие агрегатные состояния
Молекулы жидкости расположены почти вплотную, поэтому они ведут себя иначе, чем молекулы газа. Жидкости обладают свойством текучести и не имеют собственной формы. Жидкостью называется агрегатное состояние, при котором атомы (молекулы) расположены неупорядоченно, совершают перескоки из одного положения равновесия в другое. Молекулы жидкости сильно связаны с ближайшими соседями и при переходах увлекают друг друга. Твердым телом называется агрегатное состояние, при котором атомы (молекулы) расположены в строгом порядке и совершают колебания около неизменных положений равновесия. Плазмой называется агрегатное состояние, представляющее собой ионизированный, электрически квазинейтральный газ.
Таблица 1. Основные различия в агрегатных состояниях веществ
Объяснение особенностей состояний вещества на основе атомно-молекулярных представлений Особенности агрегатных состояний вещества можно объяснить на основе атомно-молекулярных представлений о расстоянии между частицами и характером их взаимодействия друг с другом. • В газе молекулы беспорядочно движутся по всем направлениям. С увеличением температуры скорость молекул возрастает. • В твердом теле молекулы практически сохраняют свое расположение, совершая лишь небольшие колебания около определенных положений равновесия. • Между молекулами жидкости действуют силы притяжения и отталкивания, что подтверждается экспериментально. Действие этих сил проявляется на расстояниях, сравнимых с размерами молекул. Жидкость принимает форму сосуда, в котором находится, при этом сохраняется её объем. Поэтому можно предположить, что молекулы жидкости могут перемещаться относительно друг друга намного свободнее, чем молекулы твердого тела. Время «оседлой жизни» молекулы воды (относительно соседних молекул), оцененное методами статистической механики, составляет примерно 10—11 с. | ||||||||||||||||||||||||||
| Просмотров: 457 | Рейтинг: 0.0/0 | ||||||||||||||||||||||||||
| Всего комментариев: 0 | |


| Лотоцкая Елена © 2024 | Сайт создан в системе uCoz
Некоторые файлы и информация, находящиеся на данном сайте, были найдены в сети ИНТЕРНЕТ, как свободно распространяемые, присланы пользователями сайта или найдены в альтернативных источниках, также использованы собственные материалы. Автор сайта не претендует на авторство ВСЕХ материалов. Если Вы являетесь правообладателем той или иной продукции или информации, и условия, на которых она представлена на данном ресурсе, не соответствуют действительности, просьба немедленно сообщить с целью устранения правонарушения. |
 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход
