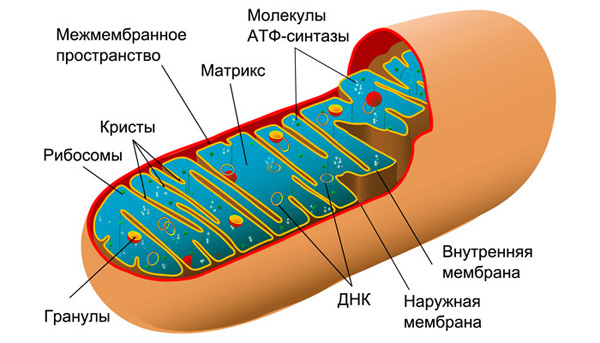
Рис. 1. Строение митохондрии. Как выяснилось, блокировка активности АТФ-синтазы и, соответственно, образования АТФ — основного источника энергии в организме — предотвращает восстановление опухоли при повторном включении онкогена KRAS. Рисунок с сайта ru.wikipedia.org
При многих устойчивых к терапии раках в опухолевых клетках наблюдается резкая активация дыхательной функции митохондрий. Ряд исследований, проведенных в последнее время, показал, что применение ингибиторов дыхательной функции митохондрий в комбинации с традиционной терапией может быть эффективно для лечения онкологических заболеваний.
Современные противораковые средства в концентрациях, практически безвредных для нормальных клеток, убивают все раковые клетки, культивируемые in vitro. Но в организме этого не происходит практически никогда. Противораковые средства эффективно убивают активно делящиеся клетки. А в организме раковые клетки могут переходить в состояние «спячки», устойчивой к терапии, пребывать в «спящем» состоянии или делиться очень медленно в течение ряда лет. «Спящие» клетки представляют собой резервуар, который может активироваться и вызвать рецидив рака. Разработка подходов, позволяющих их элиминировать, является очень актуальной проблемой. Механизмы, под действием которых раковые клетки засыпают, пока еще изучены недостаточно.
Недавно было показано (D. A. Wolf, 2014. Is Reliance on Mitochondrial Respiration a “Chink in the Armor” of Therapy-Resistant Cancer?), что специфическим свойством «засыпающих» клеток является их потребность в усилении дыхательной функции митохондрий (рис. 1). До последнего времени это свойство не использовалось при разработке подходов к лечению рака. И лишь совсем недавно большая группа ученых из Онкологического центра им. М. Д. Андерсона и других медицинских центров США и Италии пришла к выводу, что комбинация известных противораковых терапевтических средств и ингибиторов функции митохондрий может значительно повысить эффективность лечения рака (A. Viale et al., 2014. Oncogene ablation-resistant pancreatic cancer cells depend on mitochondrial function).
Исследование, показавшее эффективность комбинированной терапии, проводилось на мышиной модели аденокарциномы протоков поджелудочной железы. Это заболевание представляет собой одну из самых агрессивных форм рака, поздно диагностируется и плохо поддается лечению. Примерно половина пациентов погибает в течение 6 месяцев с момента постановки диагноза. Рак у мышей вызывали с помощью мутантного онкогена KRAS, который избирательно экспрессировался в поджелудочной железе под контролем тканеспецифичного промотора и который можно было включать и выключать. Активность мутантного онкогена необходима для инициации, роста и поддержания опухоли. После того как у животных вырастали раковые опухоли, KRAS выключали, что приводило к регрессии опухолей. Однако некоторые опухолевые клетки выживали, и через несколько месяцев развивались рецидивы.
Для детального исследования опухолевые клетки инъецировали под кожу мышам-реципиентам и при включенном KRAS подращивали подкожные опухоли (подкожные опухоли было легче исследовать, чем опухоли поджелудочной железы). Затем KRAS выключали, и опухоли деградировали. Но на месте опухолей обнаруживались выжившие остаточные эпителиоидные клетки, сходные по морфологии с клетками рака. При повторном включении KRAS подкожные опухоли быстро восстанавливались.
Следующая серия экспериментов проводилась in vitro на выращенных в полужидкой питательной среде трехмерных сфероидных культурах клеток первичной опухоли. Такие культуры представляют собой аналог опухоли in vitro. После выключения KRAS образовавшиеся сферы быстро деградировали. При повторном включении KRAS сферы, как и подкожные опухоли, быстро восстанавливались. Эффекты генетического включения-выключения KRAS воспроизводились и в экспериментах с цитотоксичными противораковыми препаратами-блокаторами онкогенных сигнальных путей.
Исследование мРНК, транскрибирующихся в клетках сфероидных культур при деградации, показало резкое усиление активности генов, связанных с функционированием митохондрий. Резко усиливалось также физиологическое проявление функций митохондрий, в том числе их главной функции — окислительного фосфорилирования (рис. 2). Обработка ингибиторами окислительного фосфорилирования полностью предотвращала восстановление сфер при повторном включении KRAS.
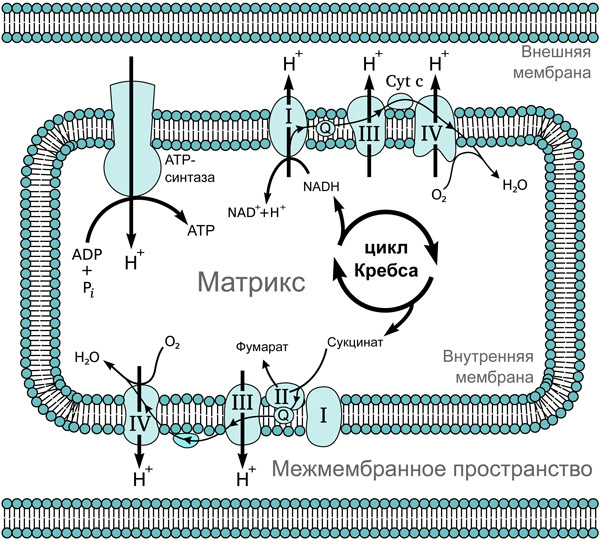
Рис. 2. Схема окислительного фосфорилирования
Рис. 2. Схема окислительного фосфорилирования. Электрон-транспортная цепь митохондрий является местом проведения окислительного фосфорилирования у эукариот. NADH и сукцинат, образовавшиеся в ходе цикла трикарбоновых кислот (цикл Кребса), окисляются, и их энергия передается АТР-синтазе, которая за ее счет синтезирует АТР. Рисунок с сайта ru.wikipedia.org
Ключевые эксперименты были проведены in vivo на мышах. Регрессия опухолей поджелудочной железы, вызванная выключением онкогенного KRAS, сопровождалась инъекциями мышам олигомицина (ингибитора окислительного фосфорилирования) в безвредных для организма концентрациях. Олигомицин блокирует последнюю стадию окислительного фосфорилирования — активность АТФ-синтазы и, соответственно, образование АТФ (аденозинтрифосфата) — основного источника энергии в организме. При последующем включении KRAS оказалось, что практически все контрольные животные погибали в течение 20 дней, но применение олигомицина значительно продлевало их жизнь, а примерно 25% мышей выживали дольше 60 дней (рис. 3).
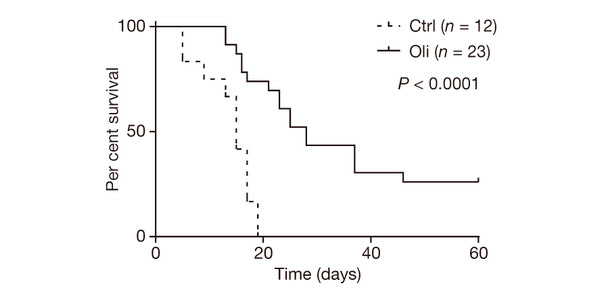
Рис. 3. Выживаемость модельных мышей после подавления опухолей и реактивации онкогена KRAS
Рис. 3. Выживаемость модельных мышей после подавления опухолей и реактивации онкогена KRAS. По оси абсцисс отложено время в днях, по оси ординат — процент выживших мышей. Сплошной линией показаны данные по мышам, которым две недели делали ежедневные инъекции олигомицина перед реактивацией KRAS (Oli); пунктиром — данные по контрольным животным (Ctrl). Рисунок из обсуждаемой статьи в Nature
Для исследования терапевтического потенциала подавления окислительного фосфорилирования применительно к раку человека сферы были получены из подкожных опухолей мышей, образованных в результате инъекции клеток аденокарциномы протоков поджелудочной железы человека. В этом случае деградация сфер вызывалась стандартными противораковыми препаратами. Обработка олигомицином до удаления этих препаратов из культуральной среды предотвращала регенерацию сфер.
Таким образом, полученные результаты позволяют считать, что подавление окислительного фосфорилирования в комбинации с традиционными средствами блокирования онкогенных путей может стать эффективным путем предотвращения рецидивов при раке поджелудочной железы. По результатам других исследований можно полагать, что такой подход может дать положительный эффект и при лечении ряда других раков. Известно достаточно много биологических маркеров, по которым можно судить о целесообразности применения этого дополнения к традиционной терапии. Но прежде чем рекомендовать ингибиторы окислительного фосфорилирования для применения в клинике, еще предстоит решить ряд вопросов. Так, нужно определить набор форм рака, при которых ингибиторы могут быть эффективны. Необходимо также найти «терапевтическое окно» — ингибиторы и их концентрации способные лечить рак, но не дающие неприемлемых побочных эффектов.
Источники: 1) Dieter A. Wolf. Is Reliance on Mitochondrial Respiration a “Chink in the Armor” of Therapy-Resistant Cancer? // Cancer Cell. 2014. V. 26. P. 788–795. 2) Andrea Viale et al. Oncogene ablation-resistant pancreatic cancer cells depend on mitochondrial function // Nature. 2014. V. 514. P. 628–632. 3) Alessia Errico. Targeted therapy: Targeting mitochondria in pancreatic cancer // Nature Reviews Clinical Oncology. 2014. V. 11. P. 562. |  Поиск
Поиск Друзья сайта
Друзья сайта Наш опрос
Наш опрос Статистика
Статистика


 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход



