| Суббота, 20.04.2024, 13:47 | Главная | Регистрация | Вход | ||||||||||||||||||||||||||||
Сайт учителя биологии и географии Лотоцкой Е. Г. |
|
||||||||||||||||||||||||||||
| « Февраль 2017 » | ||||||
| Пн | Вт | Ср | Чт | Пт | Сб | Вс |
| 1 | 2 | 3 | 4 | 5 | ||
| 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 13 | 14 | 15 | 16 | 17 | 18 | 19 |
| 20 | 21 | 22 | 23 | 24 | 25 | 26 |
| 27 | 28 | |||||
 Друзья сайта
Друзья сайта
 Наш опрос
Наш опрос
 Статистика
Статистика

14:10 Блок 1. Вещество (часть 1) | |||||||||||||||||||||||||||||
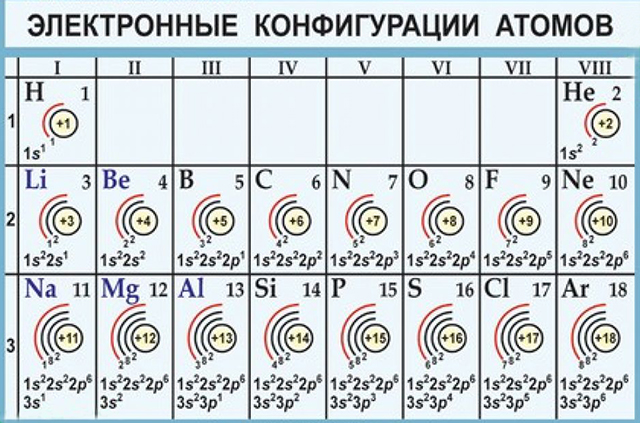
Блок 1. Вещество Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д. И. Менделеева
Нейтрон – нейтральная частица, содержащаяся в ядре. Электрон – это отрицательно заряженная частица, которая вращается вокруг ядра. В атомах одного химического элемента число протонов всегда одинаково (равно заряду ядра), а число нейтронов бывает разным. Химический элемент – это вид атомов с одинаковым зарядом ядра. Электронная оболочка – это совокупность всех электронов, вращающихся вокруг ядра. Электронное облако (орбиталь) – пространство вокруг ядра, где вероятность нахождения электрона наибольшая. Виды электронных облаков
Правила: На одной орбитали может находится не более двух электронов. Число энергетических уровней в атоме равно номеру периода. Количество электронов на внешнем энергетическом уровне равно номеру группы (для элементов главных подгрупп) Максимальное число электронов на энергетическом уровне можно вычислить по формуле 2n2
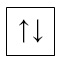
ПРАВИЛА ЗАПОЛНЕНИЯ ЭЛЕКТРОНАМИ АО, ПОДУРОВНЕЙ, УРОВНЕЙ На одной АО могут находиться только ДВА электрона, которые вращаются вокруг своей оси в противоположных направлениях (по часовой стрелке и против часовой стрелке) – электроны с противоположными спинами:
В пределах подуровня атомные орбитали заполняются одиночными электронами с параллельными спинами, и когда все орбитали данного подуровня будут заняты, происходит спаривание последних. Электроны стремятся занять энергетически выгодное положение в электронной оболочке, руководствуясь правилом наименьшей энергии расположим АО в порядке возрастания значений их энергии, которая определяется суммой: ( № УРОВНЯ + число, которое соответствует подуровню); s (0), p (1), d (2), f (3) РЯД НАИМЕНЬШЕЙ ЭНЕРГИИ 1s 2s2p 3s 3p 4s 3d 4p 5s 4d 5 p 6s 4f 5d 6p 7s 5f 6d 7p…
http://mirhim.ucoz.ru/load/0-0-0-246-20 онлайн - тест | |||||||||||||||||||||||||||||
|
|


| Лотоцкая Елена © 2024 | Сайт создан в системе uCoz
Некоторые файлы и информация, находящиеся на данном сайте, были найдены в сети ИНТЕРНЕТ, как свободно распространяемые, присланы пользователями сайта или найдены в альтернативных источниках, также использованы собственные материалы. Автор сайта не претендует на авторство ВСЕХ материалов. Если Вы являетесь правообладателем той или иной продукции или информации, и условия, на которых она представлена на данном ресурсе, не соответствуют действительности, просьба немедленно сообщить с целью устранения правонарушения. |
 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход Поиск
Поиск

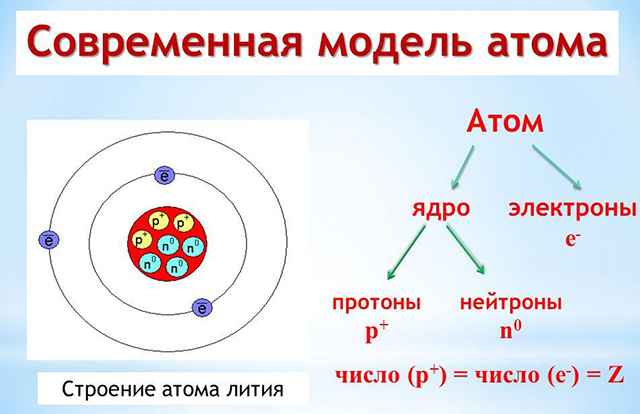
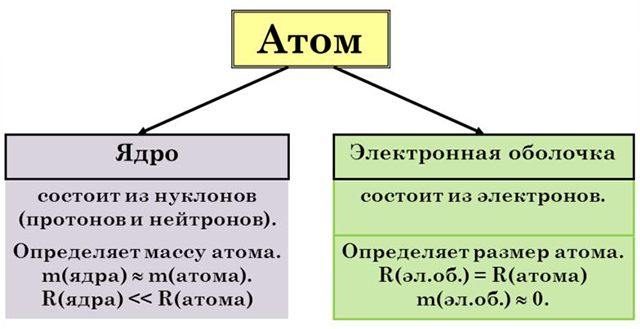 Протон – положительно заряженная частица, которая содержится в ядре.
Протон – положительно заряженная частица, которая содержится в ядре.