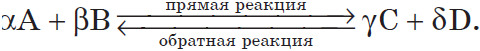Блок 1. Теоретические основы химии
1.4. Химическая реакция
1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
В зависимости от вероятности протекания реакций они подразделяются на: обратимые и необратимые. Например, реакция горения этанола практически необратимы, т.е. нельзя подобрать внешние условия, чтобы провести обратную реакцию:
2СО2 + 3Н2О = С2Н5ОН + 3О2.
Однако существует много реакций, вероятность протекания которых имеет небольшое значение. Тогда, изменяя условия процесса, можно провести процесс как в прямом, так и в обратном направлениях. Например, реакция
Н2(г) + I2(г) → 2HI(г); обратима.
В процессе реакции концентрации исходных веществ уменьшаются, а концентрации продуктов увеличиваются. Когда концентрация продуктов станет значительной, начинается обратный процесс. В результате устанавливается химическое равновесие, когда концентрации продуктов и исходных веществ остаются практически постоянными. Они называются равновесными и обозначаются в квадратных скобках, например [HI]. Химическое равновесие – равновесие динамическое.
Химическое равновесие
Большинство химических процессов являются обратимыми. Это значит, что при одних и тех же условиях протекают и прямая, и обратная реакции (особенно если речь идет о замкнутых системах).
Например:
а) реакция
t
CaCO3 → CaO+CO2↑
в открытой системе необратима;
б) эта же реакция
CaCO3 ⇄ CaO+CO2
в замкнутой системе обратима.
Рассмотрим более подробно процессы, протекающие при обратимых реакциях, например, для условной реакции:
На основании закона действующих масс скорость прямой реакции
→
υ=k1·CAα·CBβ
Так как со временем концентрации веществ А и В уменьшаются, то и скорость прямой реакции тоже уменьшается.
Появление продуктов реакции означает возможность обратной реакции, причем со временем концентрации веществ С и D увеличиваются, а значит, увеличивается и скорость обратной реакции:
→
υ=k2·CCγ·CDδ
Рано или поздно будет достигнуто состояние, при котором скорости прямой и обратной реакций станут равными
→←
υ=υ
Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, называют химическим равновесием.
При этом концентрации реагирующих веществ и продуктов реакции остаются без изменения. Их называют равновесными концентрациями. На макроуровне кажется, что в целом ничего не изменяется. Но на самом деле и прямой, и обратный процессы продолжают идти, но с равной скоростью. Поэтому такое равновесие в системе называют подвижным и динамическим.
Константа равновесия
Обозначим равновесные концентрации веществ [A],[B],[C],[D].
Тогда так как
→←
υ=υ, k1·[A]α·[B]β=k2·[C]γ·[D]δ, откуда
[C]γ·[D]δ / [A]α·[B]β = k1 / k2 =Kравн.
где γ,δ,α,β — показатели степеней, равные коэффициентам в обратимой реакции; Kравн. — константа химического равновесия.
Полученное выражение количественно описывает состояние равновесия и представляет собой математическое выражение закона действующих масс для равновесных систем.
При неизменной температуре константа равновесия — величина постоянная для данной обратимой реакции. Она показывает соотношение между концентрациями продуктов реакции (числитель) и исходных веществ (знаменатель), которое устанавливается при равновесии.
Константы равновесия рассчитывают из опытных данных, определяя равновесные концентрации исходных веществ и продуктов реакции при определенной темпера туре.
Значение константы равновесия характеризует выход продуктов реакции, полноту ее протекания. Если получают Kравн.>>1, это означает, что при равновесии [C]γ·[D]δ>>[A]α·[B]β, т. е. концентрации продуктов реакции преобладают над концентрациями исходных веществ, а выход продуктов реакции большой.
При Kравн.<<1 соответственно выход продуктов реакции мал. Например, для реакции гидролиза этилового эфира уксусной кислоты
CH3COOC2H5+H2O ⇄ CH3COOH+C2H5OH
константа равновесия
Kравн.= [CH3COOH]·[C2H5OH] / [CH3COOC2H5]·[H2O]
при 20°С имеет значение 0.28 (т.е. меньше 1). Это означает, что значительная часть эфира не гидролизовалась.
В случае гетерогенных реакций в выражение константы равновесия входят концентрации только тех веществ, которые находятся в газовой или жидкой фазе. Например, для реакции
CO2+C ⇄ 2CO
константа равновесия выражается так:
Kравн.=[CO]2 / [CO2]
Значение константы равновесия зависит от природы реагирующих веществ и темпера туры.
От присутствия катализатора константа не зависит, поскольку он изменяет энергию активации и прямой, и обратной реакции на одну и ту же величину. Катализатор может лишь ускорить наступление равновесия, не влияя на значение константы равновесия.
Смещение равновесия под действием различных факторов
Состояние равновесия сохраняется сколь угодно долго при неизменных внешних условиях: температуре, концентрации исходных веществ, давлении (если в реакции участвуют или образуются газы).
Изменяя эти условия, можно перевести систему из одного равновесного состояния в другое, отвечающее новым условиям. Такой переход называют смещением или сдвигом равновесия.
Рассмотрим разные способы смещения равновесия на примере реакции взаимодействия азота и водорода с образованием аммиака:
N2+3H2 ⇄ 2HN3 + Q
Kравн.=[NH3]2 / [N2]·[H2]3
Влияние изменения концентрации веществ
При добавлении в реакционную смесь азота N2 и водорода Н2 увеличивается концентрация этих газов, а значит, увеличивается скорость прямой реакции. Равновесие смещается вправо, в сторону продукта реакции, т.е. в сторону аммиака NH3.
Этот же вывод можно сделать, анализируя выражение для константы равновесия. При увеличении концентрации азота и водорода знаменатель увеличивается, а так как Kравн. — величина постоянная, должен увеличиваться числитель. Таким образом, в реакционной смеси увеличится количество продукта реакции NH3.
Увеличение же концентрации продукта реакции аммиака NH3 приведет к смещению равновесия влево, в сторону образования исходных веществ. Этот вывод можно сделать на основании аналогичных рассуждений.
Влияние изменения давления
Изменение давления оказывает влияние только на те системы, где хотя бы одно из веществ находится в газообразном состоянии. При увеличении давления уменьшается объем газов, а значит, увеличивается их концентрация.
Предположим, что давление в замкнутой системе повысили, например, в 2 раза. Это значит, что концентрации всех газообразных веществ (N2,H2,NH3) в рассматриваемой нами реакции возрастут в 2 раза. В этом случае числитель в выражении для Kравн. увеличится в 4 раза, а знаменатель — в 16 раз, т.е. равновесие нарушится. Для его восстановления должна увеличиться концентрация аммиака и должны уменьшиться концентрации азота и водорода. Равновесие сместится вправо. Изменение давления практически не сказывается на объеме жидких и твердых тел, т.е. не изменяет их концентрацию. Следовательно, состояние химического равновесия реакций, в которых не участвуют газы, не зависит от давления.
Влияние изменения температуры
При повышении температуры, как вы знаете, скорости всех реакций (экзо- и эндотермических) увеличиваются. Причем повышение температуры больше сказывается на скорости тех реакций, которые имеют большую энергию активации, а значит, эндотермических.
Таким образом, скорость обратной реакции (в нашем примере эндотермической) увеличивается сильнее, чем скорость прямой. Равновесие сместится в сторону процесса, сопровождающегося поглощением энергии.
Направление смещения равновесия можно предсказать, пользуясь принципом Ле Шателье (1884 г.):
Если на систему, находящуюся в равновесии, оказывается внешнее воздействие (изменяется концентрация, давление, температура), то равновесие смещается в ту сторону, которая ослабляет данное воздействие.
Сделаем выводы:
при увеличении концентрации реагирующих веществ химическое равновесие системы смещается в сторону образования продуктов реакции;
при увеличении концентрации продуктов реакции химическое равновесие системы смещается в сторону образования исходных веществ;
при увеличении давления химическое равновесие системы смещается в сторону той реакции, при которой объем образующихся газообразных веществ меньше;
при повышении температуры химическое равновесие системы смещается в сторону эндотермической реакции;
при понижении температуры - в сторону экзотермического процесса.
Принцип Ле Шателье применим не только к химическим реакциям, но и ко многим другим процессам: испарению, конденсации, плавлению, кристаллизации и др. При производстве важнейших химических продуктов принцип Ле Шателье и расчеты, вытекающие из закона действующих масс, дают возможность находить такие условия для проведения химических процессов, которые обеспечивают максимальный выход желаемого вещества. |



 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход Поиск
Поиск Друзья сайта
Друзья сайта Наш опрос
Наш опрос Статистика
Статистика