| Суббота, 20.04.2024, 14:46 | Главная | Регистрация | Вход | |||||
Сайт учителя биологии и географии Лотоцкой Е. Г. |
|
|||||
| « Апрель 2024 » | ||||||
| Пн | Вт | Ср | Чт | Пт | Сб | Вс |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 15 | 16 | 17 | 18 | 19 | 20 | 21 |
| 22 | 23 | 24 | 25 | 26 | 27 | 28 |
| 29 | 30 | |||||
 Друзья сайта
Друзья сайта
 Наш опрос
Наш опрос
 Статистика
Статистика

| ОГЭ по биологии |
| ОГЭ по географии |
| ОГЭ по химии |
| ЕГЭ по биологии |
| ЕГЭ по географии |
| ЕГЭ по химии |
|
Блок 1. Вещество Атомы и молекулы. Химический элемент. Простые и сложные вещества Химический элемент – это атомы одного и того же вида. Так, например, все атомы водорода – это элемент водород; все атомы кислорода и ртути – соответственно элементы кислород и ртуть. По элементному составу различают простые вещества, состоящие из атомов одного элемента (H2, O2,Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O,NH3, OF2, H2SO4, MgCl2,K2SO4). В настоящее время известно 115 хими ... Читать дальше » |
|
Блок 2. Химическая реакция Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях. Классификация реакций ХИМИЧЕСКИМИ ЯВЛЕНИЯМИ называют такие явления, при которых одни вещества превращаются в другие. ОТЛИЧИЯ ХИМИЧЕСКИХ РЕАКЦИЙ ОТ ФИЗИЧЕСКИХ ЯВЛЕНИЙ При физических явлениях происходит изменение формы, размера тела или агрегатного состояния вещества, но не меняется состав веществ, а при химических явлениях из одних веществ образуются другие, новые. ПРИЗНАКИ ХИМИЧЕСКИХ РЕАКЦИЙ:
|
|
Блок 2. Химическая реакция Электролиты и неэлектролиты. Катионы и анионы. Электролитическая диссоциация кислот, щелочей и солей (средних). Реакции ионного обмена и условия их осуществления ЭЛЕКТРОЛИТЫ Это вещества, растворы и расплавы которых проводят электрический ток. ИОНЫ - заряженные частицы: Cl-, Cu2+, NO3- КАТИОНЫ – ионы с зарядом + АНИОНЫ – ионы с зарядом – СВОЙСТВА ИОНОВ ОТЛИЧАЮТСЯ ОТ СВОЙСТВ АТОМОВ, ИЗ КОТОРЫХ ОНИ ОБРАЗОВАЛИСЬ!!! Процесс распада электролитов на ионы в процессе растворения или расплавления называется ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИЕЙ. ЭЛЕКТРОЛИТЫ: Все растворимые вещест ... Читать дальше » |
|
Блок 2. Химическая реакция Окислительно-восстановительные реакции. Окислитель и восстановитель ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ Реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов. ОКИСЛИТЕЛИ - это атомы, ионы или молекулы, которые ПРИНИМАЮТ электроны (степень окисления понижается). Окислитель принимает электроны – это процесс ВОССТАНОВЛЕНИЯ. Типичные окислители: 1) Оксиды, кислоты, соли с максимально положительной степенью окисления входящего в них элемента. Например: кислоты – HNO3, H2SO4, HClO4, H2Cr2O7; соли – KСlO4, KClO3, KNO3, KMn ... Читать дальше » |
|
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Химические свойства простых веществ-металлов Металлы (от лат. metallum – шахта, рудник): группа элементов, обладающая характерными металлическими свойствами. СТРОЕНИЕ АТОМА Металлы имеют большой атомный радиус и малое число электронов (от 1 до 3) на внешнем слое. Исключение: Ge, Sn, Pb ─ 4 электрона; Sb, Bi ─ 5 электронов; Po ─ 6 электронов Ме – одноатомны: & ... Читать дальше » |
|
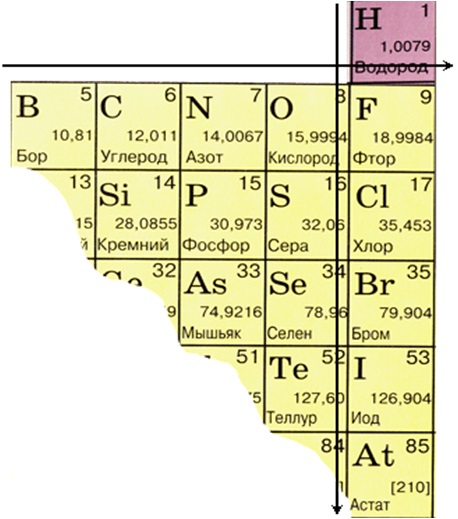
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Химические свойства простых веществ-неметаллов НЕМЕТАЛЛЫ
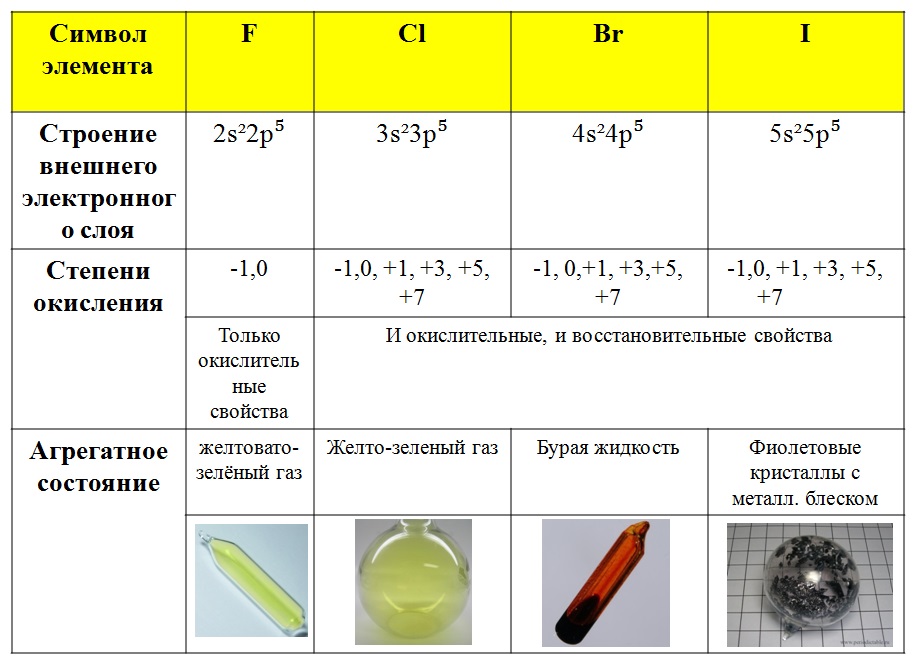
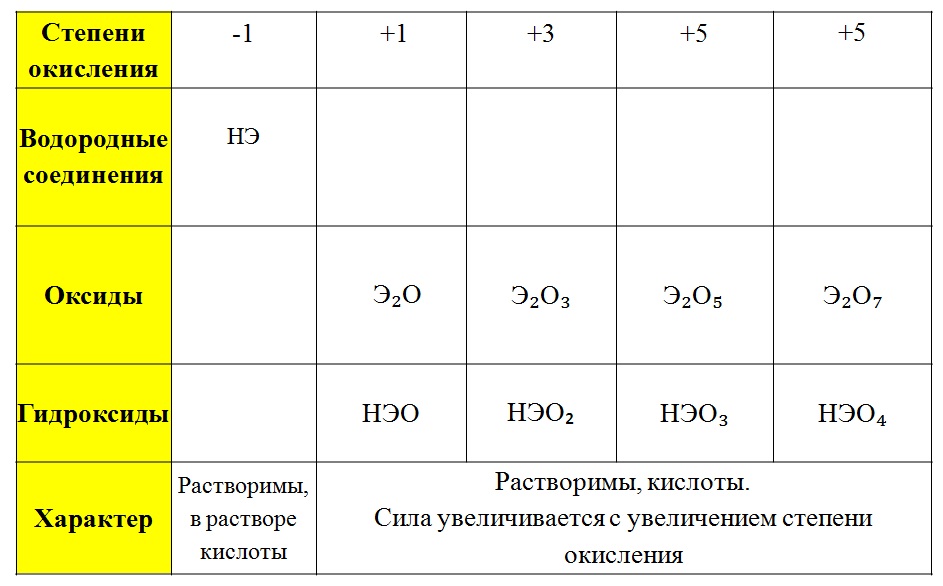
ГАЛОГЕНЫ
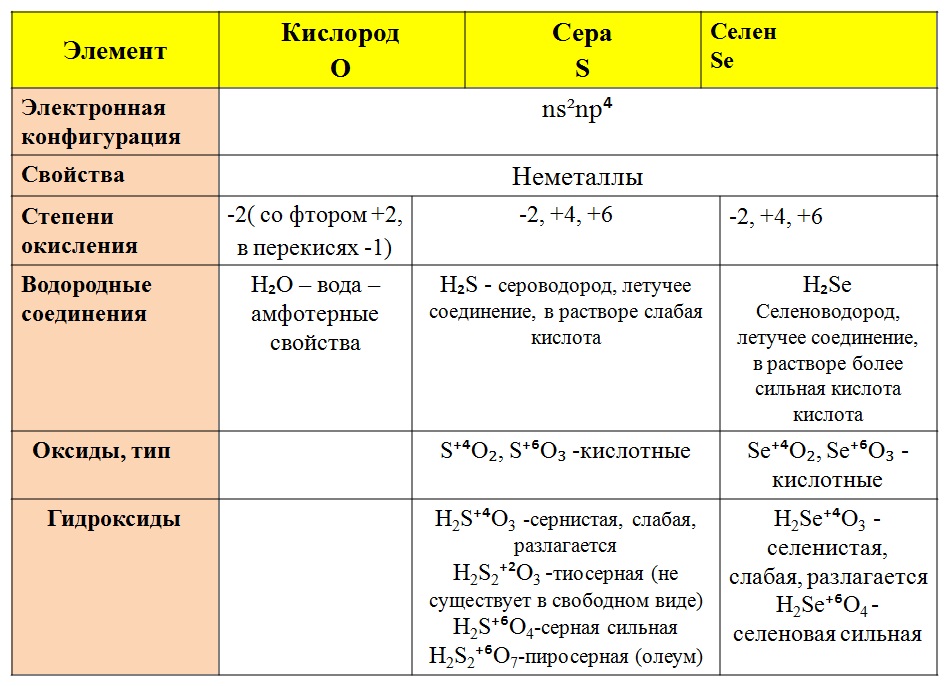
ПОДГРУППА КИСЛОРОДА Входят элементы: кислород, сера, селен, теллур, полоний.
V ГРУППА А ... Читать дальше » |
|
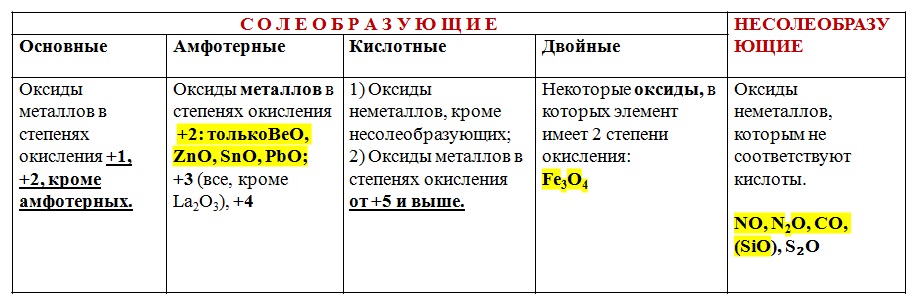
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Химические свойства оксидов: основных, кислотных, амфотерных
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВНЫХ ОКСИДОВ 1. Основной оксид + кислота (образуется соль + вода) Кислоты должны существовать в виде раствора (не реагируют кремниевая, сероводородная, угольная) Li2O + 2HCl= 2LiCl+ H2O, NiO + H2SO4 = NiSO4 + H2O 2. Основный оксид + вода (образуется щелочь) В реакцию вступают только 8 оксидов: IA группа, СаО, SrO, ВаО) Оксид реагирует с водой только если в результате образуется растворимый гидроксид (щелочь). < ... Читать дальше » |
|
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Химические свойства оснований и кислот ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ Основания – сложные вещества, содержащие в своем составе гидроксид-ионы (-ОН). Разделяются на растворимые и нерастворимые в воде основания. Растворимые основания (щелочи) в водном растворе диссоциируют на ионы. KOH = K+ + OH- Нерастворимые основания в водном растворе на ионы не распадаются!
ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧЕЙ 1.Меняют цвет индикаторов: Фенолфталеин (бесцветный) →малиновый ... Читать дальше » |
|
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Химические свойства солей (средних) СВОЙСТВА СРЕДНИХ СОЛЕЙ 1.СОЛЬ(1)+ ЩЁЛОЧЬ →СОЛЬ(2) + ОСНОВАНИЕ (соль растворимая → осадок или газ) MgCl₂ + 2NaOH = 2NaCl + Mg(OH)₂↓ NH₄Cl + NaOH = NaCl + NH₃↑ + H₂O 2.СОЛЬ(1)+КИСЛОТА(1) → СОЛЬ(2) +КИСЛОТА(2) соль растворимая → осадок, если соль нерастворимая → газ Na₂SiO₃ +2HCl = 2NaCl + H₂SiO₃↓ Na₂СO₃ +2HCl = 2NaCl + H₂O + СO₂↑ 3.СОЛЬ(1) + СОЛЬ(2) → СОЛЬ(3) + СОЛЬ(4) соли растворимые, образуется осадок Na₂SO₄ + BaCl₂ = 2NaCl + BaSO₄↓ 4.СОЛЬ(1) +МЕТАЛЛ(1) → СОЛЬ(2)+МЕТАЛЛ(2) ВСЕГДА: ... Читать дальше » |
|
Блок 3. Металлы. Неметаллы. Основные классы неорганических соединений Взаимосвязь различных классов неорганических веществ Между неорганическим веществами (простыми и сложными) существует генетическая связь, основанная на их химических свойствах. Исходя из простых веществ, получают оксиды, гидроксиды, соли. Последовательность таких превращений можно представить двумя схемами: металл → основный оксид → основание → соль, например: Са → СаО →Са(ОН)2 → Са3(РО4)2; неметалл → кислотный оксид → кислота → соль, например: Р→ Р2О5 → Н3РО4 → Са3(РО4)2. Безусловно, эти схемы не отражают всей глубины и многообразия взаимоотношений неорганических веществ. С одной стороны, нельзя понима ... Читать дальше » |


| Лотоцкая Елена © 2024 | Сайт создан в системе uCoz
Некоторые файлы и информация, находящиеся на данном сайте, были найдены в сети ИНТЕРНЕТ, как свободно распространяемые, присланы пользователями сайта или найдены в альтернативных источниках, также использованы собственные материалы. Автор сайта не претендует на авторство ВСЕХ материалов. Если Вы являетесь правообладателем той или иной продукции или информации, и условия, на которых она представлена на данном ресурсе, не соответствуют действительности, просьба немедленно сообщить с целью устранения правонарушения. |
 Меню сайта
Меню сайта Категории раздела
Категории раздела Вход
Вход Поиск
Поиск